電子処方箋 導入記 (No.9)
処方箋CSVの作成 (2) と 処方箋CSV-XML作成サンプルソフトv2
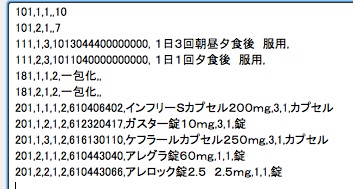
PATH5(No.5) で CSV作成のことを書きましたが,
電子処方箋管理サービス_記録条件仕様(処方編)ver1.4.pdf」とほぼ同じ内容の電子処方箋記述方法に関する文書があります。保健医療福祉情報システム工業界(JAHIS)の「医療情報交換仕様 JAHIS 院外処方箋2次元シンボル記録条件規約 v1.8」という文書です。これは処方箋CSVをQRコードで表示する仕様書ですが, 前者と同様な内容になっています。(こちらのほうが元祖でしょうか) その中に以下の図があります, 薬剤のグループごとに記載する, そのグループのなかでは 101〜281の番号順に記載するように, ということです。(前者の文書には記載がありません。)
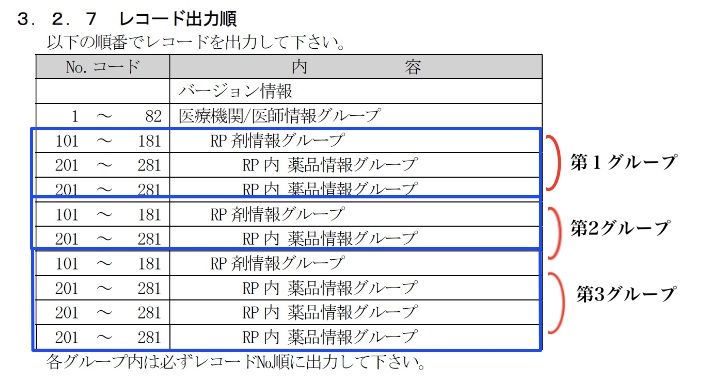
ベンダーONSに質問してみると, No5で書いたような すべて番号順に記載するやり方でもよい, ということです。確かに, No.5のCSVの行を左の2番目のグループ番号を基準に並び替えたら グループごとの記述は再現できます。サーバーに送ればあとはコンピュータがいいように処理してくれるのだと思います。
(追記: サーバーは このようなことはしないようです。前回の説明とは違って今回のONSの説明では「医療情報交換仕様 JAHIS 院外処方箋2次元シンボル記録条件規約 v1.8」に示されたとおりに記載してください, ということです。)
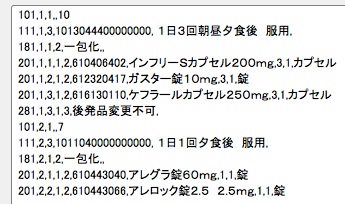
ちなみに No.5 で提示した例題を グループごとの記述にすると以下の様になります。
(後発品変更不可も追加してみました)
【般】バラシクロビル塩酸塩錠[500]/2錠/ (後発品)
アプレ−ス錠[100]/2錠/20日/朝夕内服/
(以上 一包化)
リンデロン-V軟膏[0.12%]/20g/(後発品変更不可)
プロペト/20g/1日2回塗布/躯幹/
(以上 一包化:混合外用)
【般】ロキソプロフェンNa水和物錠[60] /1錠/10回/疼痛時頓用/ (後発品)
(頓服)